제2류 위험물(가연성 고체) - 유황, 마그네슘, 철분

유황 (S, 100kg / 위험등급 Ⅰ)
순도 60% 미만의 것은 위험물에서 제외한다.
① 사방정계
㉮ 인화점은 207℃, 착화점은 232.2℃, 융점은 119℃, 비중은 2.07이다.
㉯ 산화제, 목탄가루와 혼합되었을 때 약간의 충격·가열로 착화폭발한다.
㉰ 물에 녹지 않고 이황화탄소(CS2)에 녹는다. 전기의 불량도체이다.

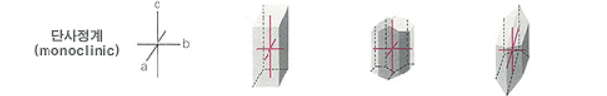
② 단사정계
㉮ 비중은 1.96이다.
㉯ 사방정계의 황을 95.5℃로 가열하여 얻는다.
㉰ 물에 녹지 않고 이황화탄소(CS2)에 녹는다.
㉱ 160℃ 에서 갈색, 250℃ 에서는 흑색으로 불투명하게 되며 유동성을 갖는다.
③ 비정계
㉮ 용융황을 물에 넣어 급랭시킨 것이다.
㉯ 물, 이황화탄소(CS2)에 녹지 않는다.
④ 황의 연소 반응식 : S + O2 → SO2(아황산가스)
아황산가스(이산화황)는 환원성의 유독한 가스이므로 호흡기를 보호해야 한다.
[예제문제]
위험물의 성질에 대한 설명 중 틀린 것은?
① 황린은 공기 중에서 산화할 수 있다.
② 적린은 KClO3와 혼합하면 위험하다.
③ 황은 물에 매우 잘 녹는다.
④ 황화인은 가연성 고체이다.
정답 : ③
마그네슘 (Mg, 500kg / 위험등급 Ⅲ)
① 착화점은 400℃ (불순물 존재 시), 융점은 651℃로, 은백색의 광택이 나는 경금속이다.
② 알루미늄보다 열전도율 및 전기전도도가 낮고, 산 및 더운 물과 반응하여 수소를 발생한다.
③ 산화제 및 할로겐 원소와의 접촉을 피하고, 공기 중 습기에 발열되어 자연발화의 위험성이 있다.
④ 소화는 마른모래나 금속화재용 분말소화약제(탄산수소염류) 등을 사용한다.
⑤ 반응식
㉮ 연소 반응식
2Mg + O2 → 2MgO(산화마그네슘) + 2 X 143.7kcal(반응열)
㉯ 탄산가스와 반응식
2Mg + CO2 → 2MgO(산화마그네슘) + C(탄소)
㉰ 온수와 반응식
Mg + 2H2O → Mg(OH)2(수산화마그네슘) + H2(수소)
㉱ 염산과 반응식
Mg + 2HCl → MgCl2(염화마그네슘) + H2(수소)
[예제문제]
위험물안전관리법령상 철분, 금속분, 마그네슘에 적응성이 있는 소화설비는?
① 불활성기체소화설비
② 할로겐화합물소화설비
③ 포소화설비
④ 탄산수소염류소화설비
정답 : ④
철분 (Fe, 500kg / 위험등급 Ⅲ)
① 회백색 금속광택을 띄며, 비교적 연한 금속분말이다.
② 주수소화를 금하고, 마른모래 등으로 피복소화한다.
③ 반응식
㉮ 염산과 반응식
Fe + 2HCl → FeCl2(염화제일철) + H2(수소)
㉯ 수증기와 반응식
3Fe + 4H2O → Fe3O4(사산화삼철) + 4H2(수소)
※ PC 버전으로 보시는 것을 추천드립니다!
부족한 글 읽어주셔서 감사합니다 :)